gewinnt.
Darmmikrobiom: sensibles Ökosystem
Lungenmikrobiom: unterschätzter Mitspieler
Auch die Lunge besitzt ein eigenes Mikrobiom – zahlenmäßig deutlich kleiner als das des Darms, aber ingesunder Lunge durch eine hohe Diversität geprägt.
In den ersten Lebensmonaten und -jahren verändert sich die Zusammensetzung des Lungenmikrobioms dynamisch. Faktoren wie Kaiserschnitt vs. vaginale Geburt, Stillen, Impfungen und frühe Infektionen prägen die Diversität.4 Eine hohe Vielfalt in der frühen Kindheit scheint protektiv zu wirken, während eine gestörte Entwicklung mit einem höheren Risiko für Asthma assoziiert ist.3
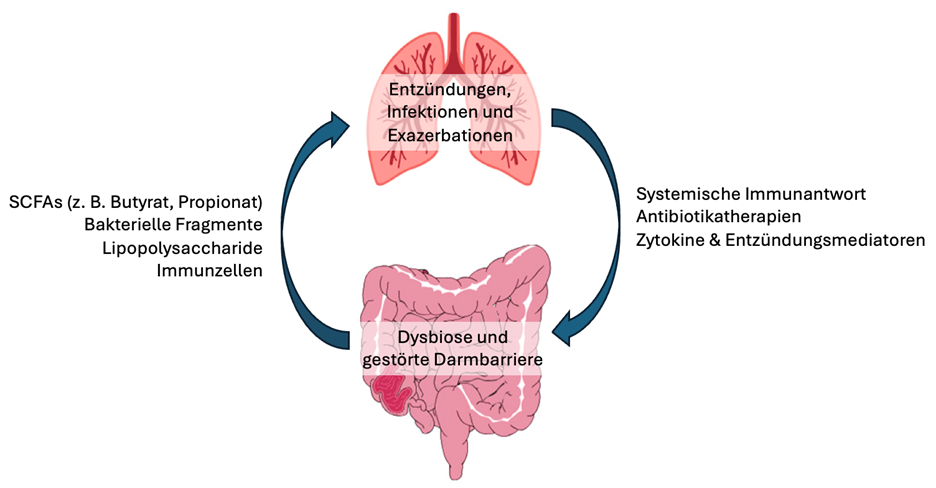
Studien zeigen, dass sich bei Asthma, COPD und anderen chronischen Lungenerkrankungen typische Muster im Lungenmikrobiom finden lassen, etwa eine Zunahme von Streptococcus und Haemophilus-Arten sowie eine Abnahme von Bacteroidetes und Actinobacteria.2 Veränderungen im Lungenmikrobiom können Entzündungsprozesse verstärken und die Immunantwort verändern. Zudem beeinflussen Dysbiosen im Darm über die Darm-Lungen-Achse auch die Zusammensetzung des Lungenmikrobioms.1,3
Asthma: frühe Prägung und Adipositas-Phänotyp
Das Darmmikrobiom beeinflusst Risiko und Verlauf von Asthma. Eine verzögerte Diversifizierung der Darmflora in den ersten Lebensjahren erhöht das Asthmarisiko. Kinder mit einem hohen Anteil butyrat- und propionatbildender Bakterien haben hingegen eingeringeres Risiko.3
Bei adipösen Asthma-Patient*innen zeigen sich charakteristische Veränderungen im Mikrobiom, die mit verstärkter systemischer Entzündung und ausgeprägterer Atemwegsreaktivität einhergehen.3 Kurzkettige Fettsäuren wirken hier als wichtige Mediatoren, die sowohl Entzündung hemmen als auch das Immunsystem regulieren.
COPD: Dysbiose verstärkt Entzündung
Bei COPD-Patienten ist eine veränderte Zusammensetzung des Darmmikrobioms häufig. Typisch sind eine reduzierte mikrobielle Diversität, ein Anstieg von Firmicutes, Prevotella und Streptococcus sowie ein Rückgang von Bacteroidetes.1,2 Diese Dysbiose kann die Darmbarriere schwächen, Lipopolysaccharide insBlut gelangen lassen und so systemische Entzündungen verstärken.1
Die Darm-Lungen-Achse beeinflusst die Krankheitsprogression: Migration von Immunzellen aus dem Darm kann Entzündungen in der Lunge antreiben oder – je nach Zelltyp – auch dämpfen.2 Klinisch relevant ist, dass eine ausgeprägte Dysbiose mit häufigeren Exazerbationen und einem schwereren Krankheitsverlauf assoziiert ist.1
Ernährung mit hohem Ballaststoffanteil, Pro- und Präbiotika sowie Fäkaltransplantationen werden erforscht. Erste Studien zeigen, dass sie Entzündungsmarker senken und die Lebensqualität verbessern könnten – aktuell jedoch nur als ergänzende Ansätze
zu leitlinienbasierter Pharmakotherapie.1,2
Das sagen die Leitlinienzu Mikrobiom und Darm-Lungen-Achse
Asthma (GINA-Report 2025)4:
- Keine Empfehlung für Mikrobiom‑gerichtete Therapien (z. B. Pro-/Prä-/Synbiotika, FMT) in der Routineversorgung; derzeit Forschungsfeld.
- Frühe Lebensfaktoren (Geburtsmodus, Stillen, Infektionen, Antibiotika) beeinflussen die Mikrobiomenentwicklungen und sind mit einem Asthmarisiko assoziiert (Hintergrund, keine Therapieempfehlung).
- Leitlinienbasierte Pharmakotherapie bleibt unverändert; Mikrobiom-Ansätze allenfalls ergänzend.
COPD (GOLD-Report 2026)5:
- Mikrobiom/Dysbiose (Darm & Lunge) und Darm–Lungen‑Achse werden als relevante Forschungsbereiche hervorgehoben.
- Keine Routineempfehlung für Mikrobiom‑Interventionen (Pro-/Prä-/Synbiotika, FMT) in der COPD-Therapie; ggf.
ergänzend/experimentell - Priorität hat die leitliniengerechte Basisversorgung (u. a. Rauchstopp, Impfungen, Bewegung, Reha, Pharmakotherapie).
Was unterstützt das Darmmikrobiom?
Lebensstilfaktoren können das Gleichgewicht des Darmmikrobioms positiv beeinflussen. Evidenz zeigt, dass eine ballaststoffreiche Ernährung – etwa mit Vollkorn, Hülsenfrüchten, Nüssen und Gemüse – die Bildung entzündungshemmender SCFAs fördert.1,2 Auch probiotische Lebensmittel wie Joghurt oder fermentiertes Gemüse können die Diversitätder Darmflora steigern.1
Omega-3-Fettsäuren sind mit antiinflammatorischen Effekten assoziiert und können die Zusammensetzung des Mikrobioms günstig beeinflussen.2 Beobachtungen aus Ernährungsstudien und translationaler Mikrobiomforschung zeigen dagegen, dass ein hoher Konsum von rotem Fleisch eher dysbiotisch und proinflammatorisch wirkt.2
Fäkale Mikrobiota-Transplantation (FMT)
Unter FMT versteht man die Übertragung von aufbereitetem Stuhl eines gesunden Spenders in den Darm, umdas Mikrobiom wieder ins Gleichgewicht zu bringen.1
Erfahrungen bisher: Erste präklinische und kleinere klinische Studien deuten darauf hin, dass FMT die mikrobielle Diversität erhöhen und systemische Entzündung senken kann.1
In COPD-Modellen zeigte sich eine mögliche Verbesserung der Lungenfunktion und Reduktion inflammatorischer Marker. Für Asthma liegen bislang nur experimentelle Daten vor, die eine Beeinflussung der Immunantwort nahelegen.3
Potenzieller Nutzen: FMT könnte künftig als ergänzende Therapieoption zur Modulation des Darmmikrobioms bei chronischen Lungenerkrankungen dienen. Leitlinien sehen den Einsatz derzeit nicht vor, FMT gilt als experimenteller Ansatz.4,5
Fußnoten
COPD: Chronisch obstruktive Lungenerkrankung;
FMT: Fäkale Mikrobiota-Transplantation;
SCFA: short-chain fatty acids
Referenzen
- Patibandla S et al. Cureus; 2024 16(8):e66875
- Song Z et al. Heliyon; 2024 10(9):e30612
- Tashiro H et al. Front Allergy; 2025 6:1618466
- The Global Initiative for Asthma (GINA). Global Strategy for Asthma Management and Prevention 2025; https://ginasthma.org/2025-gina-strategy-report/ [Abgerufen am 10.09.2025]
- Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. GOLD
Report 2026. www.goldcopd.org [Abgerufen am 27.01.2026]





Inhalt teilen