Vom 18. bis 21. März 2026 fand in München der 66. Kongress der Deutschen Gesellschaft für Pneumologie unter dem Motto „Zukunft atmen – Innovation und Menschlichkeit“ statt. Über 4.300 Teilnehmende diskutierten vor Ort in Symposien, Posterpräsentationen und Fortbildungskursenaktuelle Entwicklungen rund um Atemwegserkrankungen.
Chiesi war mittendrin – mit einem viel beachteten Symposium sowie einer Podcastreihe direkt vom Kongress. Im Folgenden haben wir für Sie die wichtigsten Inhalte zum Thema Asthma zusammengefasst. Vom 18. bis 21. März 2026 fand in München der 66. Kongress der Deutschen Gesellschaft für Pneumologie unter dem Motto „Zukunft atmen – Innovation und Menschlichkeit“ statt. Über 4.300 Teilnehmende diskutierten vor Ort in Symposien, Posterpräsentationen und Fortbildungskursenaktuelle Entwicklungen rund um Atemwegserkrankungen.
Chiesi war mittendrin – mit einem viel beachteten Symposium sowie einer Podcastreihe direkt vom Kongress. Im Folgenden haben wir für Sie die wichtigsten Inhalte zum Thema Asthma zusammengefasst.
ATEMWEG Podcast – Spezialreihedirekt vom DGP
Von Asthma bis Zystische Fibrose, von Diagnostik über Therapie bis
Versorgungspraxis – der ATEMWEG Podcast liefert regelmäßig spannende Einblicke rund um pneumologische Krankheitsbilder.
Freuen Sie sich auf aktuelle medizinische Themen, interdisziplinäre Perspektiven und authentische Gespräche mit führenden Expert*innen aus Klinik und Praxis.
Auch in diesem Jahr waren wir wieder live und exklusiv für Sie vor Ort – mit Sonderfolgen direkt vom 66. DGP-Kongress in München.
Remission durch inhalative Dreifachterapie
Um mehr über die Evidenz und die Real-World-Studie zu erfahren, loggen Sie sich einfach mit Ihrem DocCheck-Login ein.
Die multinationale, prospektive Real‑World‑Studie TriMaximize umschloss 1.422 erwachsene Patient*innen mit mittelschwerem bis schwerem Asthma, die bis zu 36 Monate beobachtet wurden.# Eingeschlossen wurden Patient*innen mit mittelschwerem bis schwerem Asthma, mit oder ohne COPD, und mit mindestens einer Exazerbation in den 12 Monaten vor Einschluss, die per ärztlicher Entscheidung leitlinien- und zulassungskonform auf eine Therapie mit der extrafeinen inhalativen Dreifach‑Fixkombination aus Beclometason, Formoterol und Glycopyrronium (Trimbow®) in mittlerer oder hoher Dosierung umgestellt wurden.1,##
„Die Daten der TriMaximize-Studie zeigen, dass die LAMA-Ergänzung zur ICS/LABA-Therapie bei mittelschwerem bis schwerem Asthma eine sehr wirksame Therapieoption darstellen kann, die leider häufig noch unterschätzt wird. Bevor bei Patient*innen der Schritt zur Biologika-Therapie erwogen wird, sollte diese Möglichkeit konsequent ausgeschöpft werden. Zumal die Daten deutlich zeigen, dass eine klinische Remission unter extrafeinem Trimbow® durchaus erreichbar sein kann.“
Priv.-Doz. Dr. med. Christian Geßner, Leipzig2
Frühe Kontrolle, weniger Exazerbationen, geringerer SCS-Bedarf
einer deutlichen und langfristigen Reduktion moderater bzw. schwerer Exazerbationen. Die verbesserte Asthmakontrolle und reduzierte Zahl der Exazerbationen spiegelt sich auch in der Anwendung der Bedarfsmedikation sowie im Bedarf an systemischen Kortikosteroiden (SCS) wider.### Die Anzahl an Patient*innen mit Bedarf an SCS hat sich innerhalb von 12 Monaten nach der Umstellung auf das extrafeine Trimbow® mehr als halbiert.1
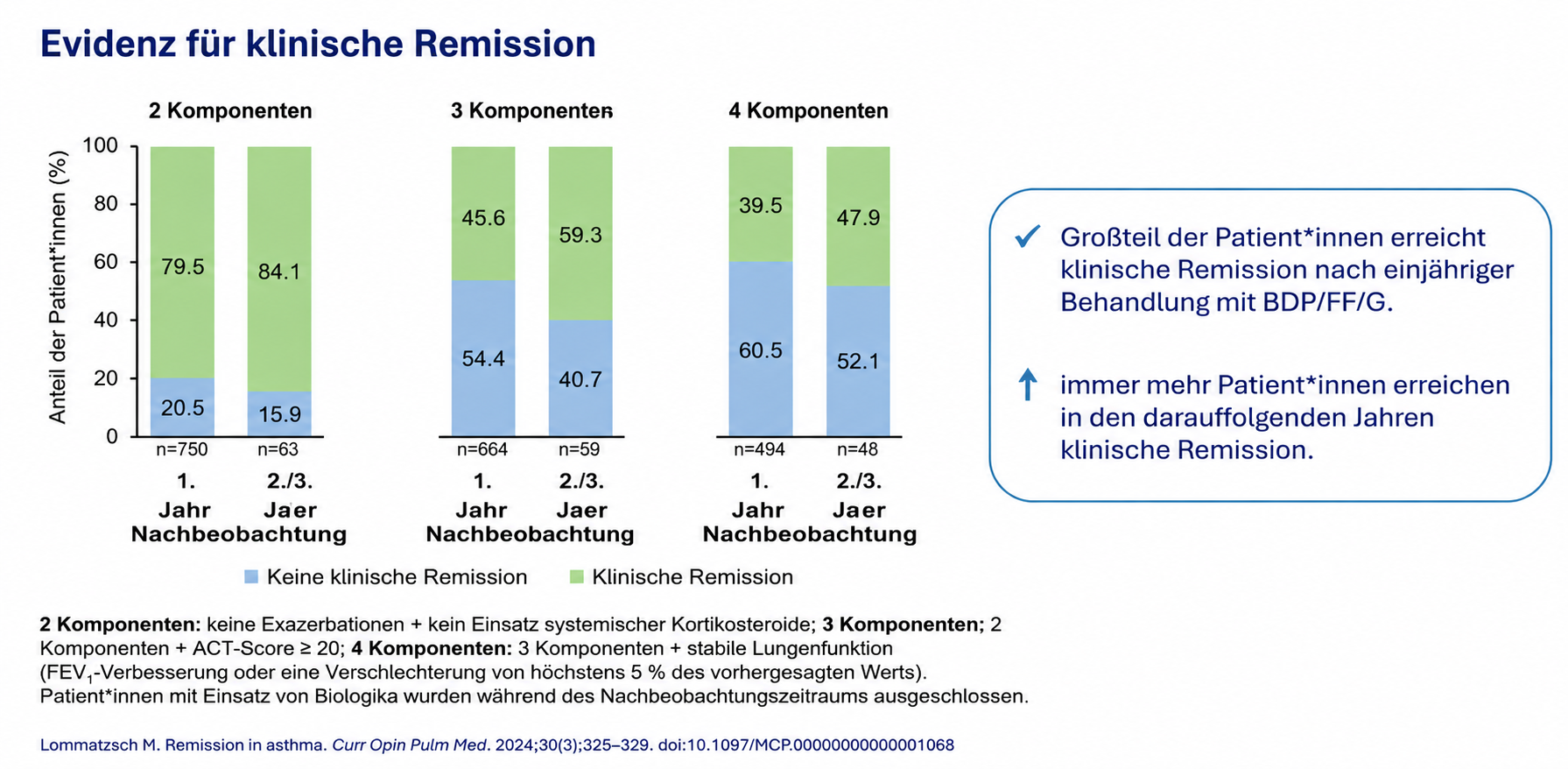
Remission unter extrafeinerinhalativer Dreifachfixkombination vergleichbar mit Biologika
Biologika bei schwerem Asthma – zunehmende Komplexität durch steigerndes Angebot
Sind Patient*innen mit schwerem Asthma (betrifft ca. 3,7 %) nach 3 Monaten unter maximaler inhalativer Triple-Therapie in ICS Hochdosis weiterhin unkontrolliert, besteht die Möglichkeit, eine Therapie mit Biologika zu initiieren.7 Aktuell gibt es in Deutschland sieben verschiedene Biologika, die für die Therapie von schwerem Asthma zugelassen sind. Dies ermöglicht eine zunehmend personalisierte Behandlung, und erhöht gleichzeitig die Komplexität im Assessment, welches Biologikum für welche*n Patient*in geeignet ist (u. a. allergisches oder intrinsisches Asthma, Biomarker,Komorbiditäten, Dosierungsintervall).8
Seit Februar dieses Jahres steht mit Depemokimab erstmals ein ultralangwirksames Biologikum zur Behandlung des Asthmas zur Verfügung, das lediglich in einem sechsmonatigen Dosierungsintervall appliziert werden muss.9,10
Pipeline-Update: inhalierbare Anti-TSLP- Fragmente und Nanobody-Therapie
OCS bei Asthma: Risiken bereits bei niedrigen Dosen
Dosen sollte der Einsatz von OCS nicht als pragmatische Dauerlösung, sondern als klares Warnsignal für eine ggf. notwendige Therapieeskalation verstanden werden.13
Hier geht´s zum Kongressbericht zu COPD
Fußnoten
# In der nicht‑interventionellen, prospektiven TriMaximize‑Studie wurden Patient*innen über einen Zeitraum von bis zu 36 Monaten beobachtet. Wie bei Langzeitbeobachtungen üblich, nahm die Zahl der auswertbaren Patient*innen im Verlauf kontinuierlich ab. Dies ist primär auf Studienabbruch, fehlende Folgedokumentationen oder unvollständige Visiten zurückzuführen und spiegelt die typische Attrition in Real‑World‑Settings wider. Die Patientenzahlen pro Visite (V) betrugen: V1/Baseline: n=1.445; V2/3 Monate: n=1.038; V3/6 Monate: n=919; V4/9 Monate: n=712; V5/12 Monate: n=800; V6/18 Monate: n=427; V7/24 Monate: n=281; V8/30 Monate: n=181; V9/36 Monate: n=63.1
## Während der Studie waren nur Umstellungen von einer vorherigen mittleren ICS-Dosis auf MS BDP/FF/G oder von einer vorherigen hohen ICS-Dosis auf HS BDP/FF/G erlaubt.1
### Vor Initiierung der BDP/FF/G‑Therapie: Systemische Kortikosteroide in den letzten 12 Monaten, Biologika in den letzten 12 Monaten, Bedarfsmedikation in den letzten 7 Tagen und Nutzung von Gesundheitsressourcen in den letzten 3 Monaten.1
#### Um sicherzustellen, dass eine Remission nicht lediglich durch eine gleichzeitige Behandlung mit Biologika erreicht wurde, wurden Patienten, die während der Nachbeobachtungszeit Biologika erhielten, von dieser Analyse ausgeschlossen.1
Referenzen
- Gessner C. et al., J Asthma Allergy2026; 19:1–21
- Pressedinner „TriMaximize: Premiere bei Evidenz zur fixen Dreifachkombination bei Asthma im Real-World-Setting“. München, 20. März 2026. Chiesi GmbH Hamburg
- Shackleford A et al. Lancet Respir Med. 2025 Jan;13(1):23-34.
- Hansen S, Chest. 2024 Feb;165(2):253-266.
- Meulmeester FL et al., Lancet Respir Med 2025; 13(6):505–516.
- The Global Initiative for Asthma (GINA). Global Strategy for Asthma Management and Prevention 2025; https://ginasthma.org/2025-gina-strategy-report/ [Abgerufen am 30.03.26] S. 140.
- Bundesärztekammer (BÄK) KBK, Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF), (2024) Nationale VersorgungsLeitlinie Asthma, Version 5.0 https://register.awmf.org/de/leitlinien/detail/nvl-002 [Abgerufen am 30.03.26]
- Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) (2023) S2K-Leitline zur fachärztlichen Diagnostik und Therapie von Asthma 2023
https://register.awmf.org/de/leitlinien/detail/020-009 [Abgerufen am 30.03.26] - GSK Pressemitteilung vom 17.02.2026 „Exdensur (depemokimab) approved by the European Commission for severe asthma with type 2 inflammation and chronic rhinosinusitis with nasal polyps”, Exdensur (depemokimab) approved by the European Commission for severe asthma with type 2 inflammation and chronic rhinosinusitis with
nasal polyps | GSK - Fachinformation EXDENSUR 100 mg Injektionslösung im Fertigpen, EXDENSUR 100 mg Injektionslösung in einer Fertigspritze. Stand Februar 2026
- O'Byrne PM, Panettieri RA Jr, Taube C, Brindicci C, Fleming M, Altman P. Development of an inhaled anti-TSLP therapy for asthma. Pulm Pharmacol Ther. 2023 Feb;78:102184.
- DGP 2026 Klinisches Symposium: Sy 78 - State of the Art Asthma." Samstag (21.03.2026), Speaker Prof. Taube
- Dreher et al. Adverse Outcomes Associated with Systemic Glucocorticoids: Dose–Time Effects in Real-World Inflammatory Disease Cohorts. Preprint Artikel verfügbar unter: https://papers.ssrn.com/sol3/papers.cfm?abstract_id=6201892
[Abgerufen am 02.04.26]






Inhalt teilen